联 系 人:吉恩特客服
手 机:136-0866-9917(微信同号)
地 址:河南省洛阳市高新区火炬创业园
近日,肝癌早筛研究传来好消息,中国浙江大学医学院和郑州大学***附属医院的研究人员联合在《BMJ》子刊《Gut》上发表了一篇重磅文献,他们成功建立了肝癌早期筛查模型!而且,这个模型还跟***近发展得如火如荼的肠道菌群联系起来了!
肝癌之所以难治、死亡率高,重要缘由之一就是早筛极为困难,其早期症状不明显,容易与其他疾病混淆,导致大多数患者错过了***佳治疗时机,因此,解决肝癌早筛困难的问题尤为重要。我们知道,肿瘤早筛早诊的关键是建立一个有效的检测模型,借此寻找作为筛查与诊断的标记。
而检测模型的建立,***重要的是一定要保证每个患者都带有这些标记,否则模型的适用度就会大打折扣。同时,涉及普及度,还要将标记获取途径的难易纳入考虑范围。如何同时兼顾这些问题呢?研究人员将目光投向了我们日常排泄物之一—粪便,而其中的肠道菌群变化,正是早筛的重要标准。
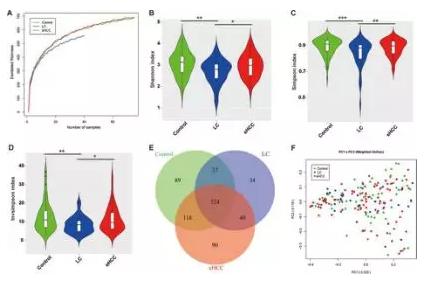
肝硬化患者肠道菌群多样性降低
此次,研究人员收集了华东、华中和西北地区的486份粪便样本,这些样本包含了健康人、肝硬化患者、早期肝癌患者,他们对其中419份样本进行了Miseq测序,并对测序结果进行队列分析。
他们发现,相较于健康人和早期肝癌患者,肝硬化患者的肠道菌群多样性竟然是***低的!而健康人和早期肝癌的肠道菌群多样性也有极大不同!也就是说,这三种人群可以直接通过肠道菌群分析轻易辨别!
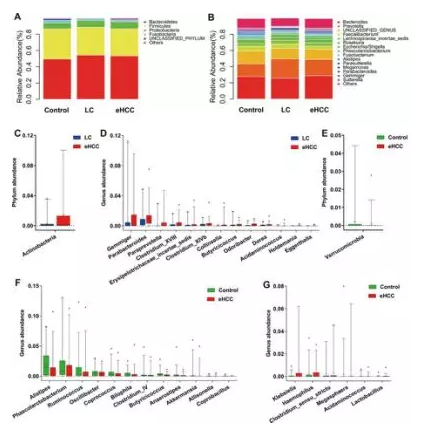
早期肝癌患者肠道菌群变化
肝癌、肝硬化究竟有哪些特殊的肠道菌群变化呢?研究人员发现,与肝硬化患者相比,早期肝癌患者肠道内包含Gemmiger、Parabacteroides等13个属的放线菌明显富集。
另外,早期肝癌患者产丁酸盐属细菌减少,产脂多糖属细菌增加。这就说明从肝硬化到肝癌,肠道微生物群发生了显着的转变,并且改变的微生物群落可能在肝癌启动和发展过程中发挥重要作用。
那么这些肠道菌群干了什么呢?首先,放线菌是***的致病菌,可明显恶化肠道环境,破坏机体稳态。其次,丁酸盐是肠粘膜的主要能量来源,是宿主细胞中基因表达、炎症、分化和凋亡的重要调节因子,在细菌能量代谢和肠道健康中起着关键作用。
产丁酸盐细菌的减少会导致肠粘膜破坏,使肝癌恶化。而产脂多糖细菌的增加将引发各种病理生理级联反应。高水平的脂多糖可激活NF-κB通路,产生促炎细胞因子(TNF-α,IL-6和IL-1),导致肝脏炎症和氧化损伤,从而促进肝癌的发展。也就是说,这些菌群变化,都可以成为衡量肝癌发展的标准!

随机森林模型的微生物标记
但是,仅靠以上几种菌群变化尚不足以准确筛查肝癌,这些菌群变化与其他疾病有所重叠,因此,需要更多菌群变化信息共同作为筛查标准。研究人员根据测序结果,构建了一个随机森林(random forest)模型,其中包含了30个***能准确反映肝癌进程的微生物标记。
这个模型筛查早期肝癌的AUC(AUC用来判断预测模型的优劣,越接近1,说明预测越准确)值达到了80.64%!在中国西北和中部的肝癌的跨区域验证中,这个模型区分健康人和早期肝癌患者的AUC值为76.80%,区分健康人与晚期肝癌患者的AUC值达到了80.40!也就是说,这个模型对晚期肝癌的筛查同样有效!
这个模型将肠道菌群变化与肝癌筛查紧密联系起来,有望成为早期肝癌诊断的有效非侵入性工具,这对笼罩在肝癌阴影下的人们是莫大的好消息,这也是我国科学家们对肝癌研究的重大贡献。