联 系 人:吉恩特客服
手 机:136-0866-9917(微信同号)
地 址:河南省洛阳市高新区火炬创业园
去年7月,AlphaFold预测出98.5%的人类蛋白结构;现在,AlphaFold又站上了药物研发的战线。其预测的结构可以促进基于结构的药物设计,特别是对于那些缺乏足够的蛋白结构信息的新靶点。
近日,英矽智能公司的研发团队就借助AlphaFold,针对一个缺乏可用蛋白结构信息的新型靶点,开发出潜在的全球首创(first-in-class)苗头化合物。目前该论文已上传***arXiv预印本平台。
在这项工作中,研发团队将AlphaFold应用于英矽智能开发的端到端AI药物发现引擎中,这个引擎由生物计算平台PandaOmics和生成化学平台Chemistry42组成。
其中,PandaOmics以来自组学和文本数据的信息为起点,将AI深度学习和生物信息学方法相结合,用于数据的分析、可视化和解读,判定基因与疾病靶点的关联性,从而找到有潜力的靶点。
不过,如果这些靶点没有明确的晶体结构,传统方法将难以继续开展研究。这时,AlphaFold的作用就体现了出来:它能够准确地预测蛋白结构,这样研究者就可以选择***具潜力的靶点,运用Chemistry42 平台设计苗头化合物。
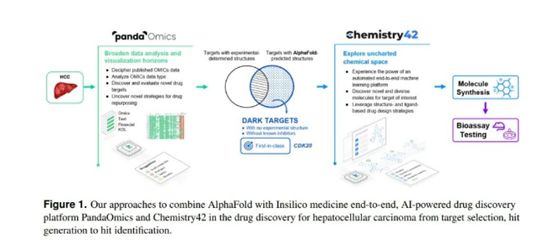
▲研发团队将 AlphaFold与英矽智能的AI药物发现平台 PandaOmics 和 Chemistry42 相结合,针对肝细胞癌进行靶点发现与苗头化合物的设计和生成。
在这项研究中,这个引擎寻找的是针对肝细胞癌的靶点。根据国际癌症研究机构 (IARC) 发布的全球癌症(GLOBOCAN)统计报告2020年版,原发性肝癌是全球第六大常见癌种,也是癌症死亡的第三大原因。肝细胞癌 (HCC) 是肝癌的主要类型,约占患者总人数的 75%。由于预后不佳,全球范围内肝癌的死亡率和发病率不相上下。
为了寻找治疗靶点,研发团队首先获取了包含1133 个患者样本和 674 个健康样本的肝细胞癌数据集。利用这些数据,PandaOmics筛选出20个有潜力的靶点。由于AlphaFold已经预测出这些靶点的晶体结构,PandaOmics可以基于靶点与疾病的关联度给出评分。这样,作者确定了得分***高的靶点——细胞周期蛋白依赖性激酶20(CDK20)。
已有研究发现,CDK20在结直肠癌、肝细胞癌、肺癌和卵巢癌等多种癌症患者的肿瘤样本中过度表达。这个分子通过多种方式促进肿瘤细胞的生长与增殖:它们不仅参与调节肿瘤细胞周期和致癌信号传导,还与某些肿瘤的免疫抑制相关。因此,尽管发现的时间不长, CDK20已经引起了广泛关注。CDK20 抑制剂一旦问世,将有望成为癌症,特别是肝细胞癌的创新疗法。
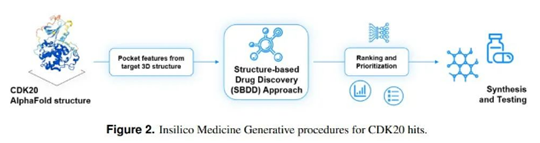
▲英矽智能针对CDK20靶点的苗头化合物生成过程
但遗憾的是,尽管针对CDK家族其他部分成员的药物研发大获成功(例如多款CDK4/6抑制剂已经获批上市,用于治疗乳腺癌、肺癌等),但针对CDK20抑制剂的研发尚未出现。一个重要原因就在于,CDK20没有可用的蛋白结构信息。在这项***新研究中,基于Alphafold 预测的蛋白结构,Chemistry42成功设计、生成了潜在的CDK20 抑制剂。
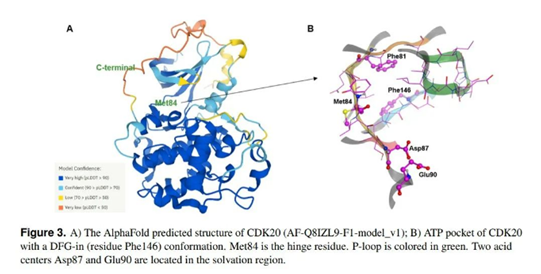
▲A) CDK20的 AlphaFold 预测结构;B) CDK20 的 ATP 结合口袋
Chemistry42从预测的蛋白结构中发现,CDK20有一个较浅的ATP结合口袋。结合这个口袋的结构特性,Chemistry42设计并生成了8918种分子结构,并且***终筛选出7个***具潜力的化合物进行合成。
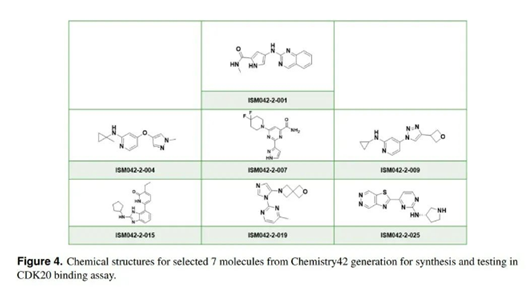
▲Chemistry42生成的7 个分子的化学结构
通过进一步的评估,研发团队发现在7个候选化合物中,化合物ISM042-2-001与CDK20结合的能力极强。研发团队随后预测了其结合模式,基于这一模式,研发团队目前正在对ISM042-2-001进行更多衍生物的设计与合成,以进一步提高酶活性。
在这篇论文里,研发团队展示了将AlphaFold与AI引擎PandaOmics和Chemistry42相结合,在30天内完成了靶点选择、分子生成、化合物合成和生物学测试,***终快速发现有望治疗肝细胞癌的苗头化合物分子。目前,对该分子的进一步优化仍在进行中。这项研究也是将 AlphaFold 预测的蛋白结构用于药物研发的一个实例,之后英矽智能也会继续公布对其他靶点类型(如GPCR和E3连接酶)的进一步研究。
生物磁珠对细胞筛选的方法已日渐成熟,原理是将包被一抗的磁珠与细胞表面对应的分子特异性结合,或者将包被二抗的磁珠与已经与细胞表面分子特异性结合的一抗结合。磁珠携带与之结合的细胞吸附与分离柱或试管上,实现阳性细胞或阴性细胞的分离。洛阳吉恩特生物自主研发生产了各类生物磁珠,可以实现稳定的实验结果。