联 系 人:吉恩特客服
手 机:136-0866-9917(微信同号)
地 址:河南省洛阳市高新区火炬创业园
在过去十年里,基于CRISPR的基因编辑技术得到了快速发展,并被成功应用放到了人体临床试验中已治疗遗传疾病和癌症。与此同时,全世界的科学家们也在不断挖掘新的具有基因编辑潜力的新工具,以解决现有基因编辑工具尺寸太大难以被单个AAV载体递送的问题。
张锋团队在 Science 期刊发表论文【1】,发现了一类广泛的转座子编码的RNA引导核酸酶,并将其命名为OMEGA系统(包括IscB、IsrB、Tnp8),它们同样使用一段RNA(ωRNA)来指导切割DNA双链。
其中IscB被认为是Cas9的祖先,更重要的是,IscB非常小,大约400个氨基酸,仅为Cas9的约30%,这意味着它们可被开发为新的小型化基因编辑工具,从而更容易被递送到细胞内。之后,张锋、可爱龙等人发表了了一系列论文,解析了IscB-ωRNA的结构,及其切割DNA的机制。
杨辉团队在 Nature Methods 期刊发表了题为:Development of miniature base editors using engineered IscB nickase 的研究论文。
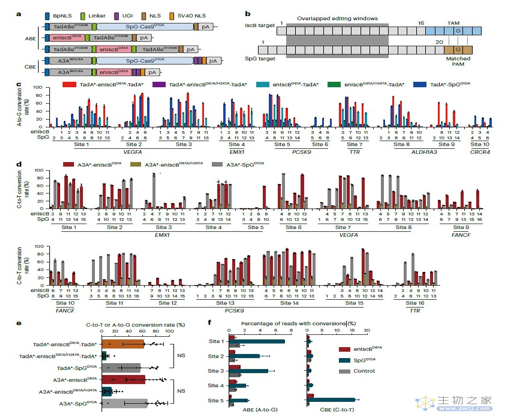
该研究对IscB进行了大量优化和改造,获得了在人类细胞中具有***基因编辑活性的IscB变体——enIscB。将enIscB切口酶分别与腺苷脱氨酶和胞苷脱氨酶结构域融合,进一步开发出了迷你型碱基编辑器——miABE和miCBE。这些迷你型碱基编辑器在真核细胞中显示出强大的单碱基编辑效率,***高可达92%。

作为一种小型的由RNA引导的核酸酶,IscB被认为是Cas9的祖先,并具有与Cas9相似的功能。而IscB的大小不到Cas9的一半,因此更适合使用腺相关病毒(AAV)载体进行体内递送。然而,IscB在真核细胞中的编辑效率较低,这***了其在体内的应用。
在这项研究中,研究团队对在哺乳动物细胞中具有微弱编辑活性的OgeuIscB及其ωRNA进行了工程化设计,进而开发出了一个在哺乳动物系统中***编辑活性的IscB变体,并将其命名为enIscB。
接下来,研究团队将enIscB与T5核酸外切酶(T5E)融合,发现enIscB-T5E在人类细胞(HEK293)基因组中具有与SpG Cas9相当的靶向切割效率,同时表现出较低的染色体易位效应。
研究团队在enIscB的基础上,进一步改造和筛选到了enIscB切口酶(enIscB nickase),将其分别与腺苷脱氨酶或胞苷脱氨酶结构域融合,开发出了迷你型碱基编辑器(miBE)——miABE和miCBE,这些迷你型碱基编辑器在真核细胞中显示出强大的单碱基编辑效率,***高可达92%。
总的来说,该研究建立了enIscB-T5E和miBE作为基因组编辑的通用工具。更重要的是,miBE不仅具有高碱基编辑活性,还具有迷你尺寸的有点,有助于解决当前碱基编辑工具太大而无法被单个AAV载体递送的难题,为体内碱基编辑的应用带来了新的可能性。
核酸提取磁珠作为新冠病毒RNA提取的重要原料,是吉恩特生物自主研发生产的高分子材料,将均一的分子材料的粒径控制在合理的范围内,加入磁性,再引入配基,从而使分子材料具备磁响应性和生物吸附性能,在核酸提取的过程中可以得到良好的应用,尤其是GNT-108磁珠,更是对新冠病毒的RNA提取具有较高的特异性,提取结果可直接应用与下游定量检测。