联 系 人:吉恩特客服
手 机:136-0866-9917(微信同号)
地 址:河南省洛阳市高新区火炬创业园
癌症背后的分子机制一直是科学研究的热点。在癌症的众多驱动因素中,TP53基因被誉为“基因组的守护者”,是人类体内***重要的肿瘤抑制基因之一。然而,这位“守护者”也常常成为癌症发展的“叛徒”,数据显示,大约50%的癌症患者都携带TP53基因的突变。这些突变不仅破坏了基因的抑癌功能,还可能赋予癌细胞更强的生存和增殖能力。但遗憾的是,尽管已经记录了超过2000种TP53错义突变,绝大多数仍然是“未解之谜”。
为了深入探究这些突变的功能多样性,Nature Genetics的研究报道“Deep CRISPR mutagenesis characterizes the functional diversity of TP53 mutations”,利用CRISPR基因编辑技术,系统性地筛选了9225种TP53基因变体。这项研究的独特之处在于,其分析范围覆盖了94.5%的癌症相关突变,为***解读这些突变对癌细胞生物学行为的影响提供了***的高分辨率视角。研究发现,这些突变在细胞生长、凋亡以及对药物的反应中展现出了显著的功能差异,甚至揭示了一些潜在的药物靶点,为个性化治疗带来了新的希望。
此外,该研究不仅在功能丧失(Loss of Function, LOF)的变体中发现了令人瞩目的规律,还***揭示了一些看似无害的突变如何通过改变RNA剪接或引发无义介导的RNA降解(NMD),间接破坏基因功能。这样的发现,不仅使我们对TP53突变的理解更加深入,也为癌症的早期诊断和靶向治疗带来了新的契机。 
基因组的守护者:TP53的重要角色
TP53基因被誉为“基因组的守护者”,这个称号不仅源于它的重要性,更因为它在细胞生命活动中的独特地位。作为一个编码p53蛋白的基因,TP53通过一系列机制保护我们的基因组稳定性,为细胞筑起了抵御癌变的***道防线。p53是一种关键的转录因子,当细胞受到DNA损伤、氧化应激或其他压力时,它会迅速启动一系列防御反应,包括细胞周期停滞、细胞衰老和程序性细胞死亡(apoptosis)。这些机制旨在修复受损DNA,或者在损伤无法逆转时“牺牲”受损细胞,防止癌症的发生。
然而,p53的功能远不止于此。研究发现,p53还参与调控细胞代谢、炎症反应和基因组复制的完整性,这使得它在肿瘤抑制之外具有更多的生理意义。例如,当细胞处于能量缺乏或营养匮乏的情况下,p53能够通过调节代谢途径,帮助细胞适应压力环境。这种全方位的守护功能使得TP53基因成为进化过程中高度保守的基因之一。
有趣的是,p53的作用并不是“独唱”,而是与多种蛋白质密切协作完成的。例如,MDM2是一种与p53关系密切的蛋白,通过对p53的降解调节其活性。在正常细胞中,p53水平被严格控制,以避免不必要的细胞死亡或生长停滞。但当细胞受到压力时,这种控制机制被迅速打破,p53被激活,从而扮演起基因组“守护者”的角色。
这种复杂而精密的调控网络使TP53成为癌症研究的核心。然而,这位守护者也极其“脆弱”。一旦TP53基因突变,其保护功能可能完全失效,甚至反过来促进肿瘤发展。由此可见,TP53不仅是基因组稳定性的守护者,也是理解癌症发生机制的关键窗口。
尽管TP53基因在正常细胞中扮演着“基因组守护者”的角色,它也可能成为癌症发生的关键驱动因素。当TP53基因发生变异时,p53蛋白的肿瘤抑制功能可能完全丧失,甚至被“劫持”,赋予癌细胞更强的生存优势。据统计,大约50%的癌症患者都携带TP53基因突变,这使其成为癌症研究领域***具影响力的基因之一。
TP53突变的绝大多数是错义突变(missense mutations),其中90%以上集中在p53的DNA结合域(DBD)。这个区域对于p53的功能至关重要,其突变不仅会削弱p53识别和调控目标基因的能力,还可能导致细胞生长失控和肿瘤的形成。例如,研究中发现的R175H、R248Q等“热点”突变,能够显著增强癌细胞的增殖和侵袭能力。而在临床上,携带这些突变的患者往往预后较差,显示出其强大的致癌潜力。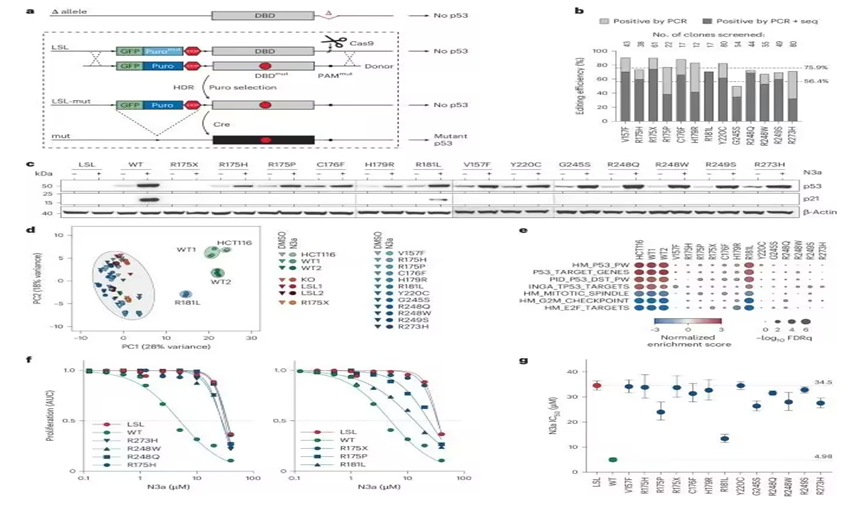
HCT116细胞系中单一TP53突变的功能解析(Credit: Nature Genetics)
更复杂的是,有些TP53突变不仅会导致功能丧失(Loss of Function, LOF),还会获得新的致癌特性(Gain of Function, GOF)。这些突变体可以通过重新编程细胞信号通路,促进肿瘤的侵袭和转移。例如,某些变异的p53蛋白可以与正常的p53蛋白竞争,形成失活的复合体,或与其他蛋白质结合,干扰细胞的正常功能。这些“获得功能”的突变可能让肿瘤更具侵略性,也更加难以治疗。
此外,TP53突变还常常伴随其他遗传和表观遗传改变,如染色体倍体异常和基因组不稳定性,这些二次改变进一步加速了肿瘤的发生和发展。研究中通过CRISPR技术筛选的9225种TP53变体表明,功能丧失的突变在癌症中尤为常见,部分突变还可能通过剪接异常或无义介导的RNA降解(NMD)机制进一步失去功能。
ctDNA的提取在肿瘤筛查中,是重要的前置步骤。目前常用的提取方法是利用生物磁珠,主要是硅羟基磁珠或羧基磁珠对血清血浆的ctDNA进行提取,由于磁珠的粒径小,比表面积大,在特定提取缓冲液中,对核酸的吸附会更加灵敏,相比于其他方法,使用生物磁珠对进行ctDNA提取得率会更高,检测灵敏度和检出限也会更合适,搭配核酸提取仪,更能实现全程自动化的提取。