联 系 人:吉恩特客服
手 机:136-0866-9917(微信同号)
地 址:河南省洛阳市高新区火炬创业园
对于侵袭性 B 细胞淋巴瘤,实现缓解是迈向治愈的***步,PET/CT扫描之类的放射影像学检查是目前确定治疗结束时缓解情况的标准方法,但其对淋巴瘤缺乏特异性,且无法在分子水平上检测疾病。如果能通过超灵敏检测循环肿瘤DNA(ctDNA)来识别可测量残留病(MRD),则有可能改善临床结局。
侵袭性 B 细胞淋巴瘤中ctDNA 的早期研究显示,其与总体肿瘤负荷有很强的关联,且基线ctdNA定量与一线化疗后的临床结局相关。检测ctDNA 中淋巴瘤相关基因异常的下一代测序也可用于进行非侵入性的基因分型,其结果与组织活检高度一致。一线化疗1或2个周期后或CAR-T 细胞挽救治疗数周内循环肿瘤 DNA 的动态变化也具有很强的预后价值。尽管ctDNA 的连续监测可在临床复发前 3 至 6 个月检测到分子学复发,但若要在治疗结束时单次检测到MRD,仍需提高分析阈值。现代ctDNA 方法的进步现已能够可靠地检测MRD,其分析检测阈值为100万分之一的游离 DNA 分子。
现代超灵敏检测ctDNA 的方法可能会改善侵袭性 B 细胞淋巴瘤目前对缓解的定义。在治疗结束评估时纳入ctDNA 可以识别出无需监测随访的患者,并在临床试验中引入治疗可测量残留病的新模式。但ctDNA的应用也面临很多障碍,包括收集标准化、可获得性、周转时间和成本,仍是阻碍其在临床实践中广泛应用的障碍。
《JAMA Oncology》近日发表重磅综述,阐述了循环肿瘤DNA在侵袭性B细胞淋巴瘤MRD评估中的作用。 
当前的缓解评估
侵袭性 B 细胞淋巴瘤是***早被证实通过化疗可能治愈的癌症之一,在一线治疗中加入多柔比星和利妥昔单抗后,治愈率得到显著提高。如果希望实现治愈,首先必须经历缓解,从概念上讲,缓解是指在治疗结束时(EOT)体内没有活跃淋巴瘤,然而确切地定义缓解一直是个难题。CT的出现是一项重要进步,它增强了对全身疾病进行可视化的能力,并确定了疾病的解剖位置,尤其是在淋巴结区域。然而CT 扫描在 EOT 时定义缓解的局限性很快就显现出来,因为许多侵袭性淋巴瘤患者在治疗后仍有残留肿块,但在长期随访中并未复发。CT 扫描的不精确性反映在***初制定的共识反应标准中,治疗后仍有残留肿块但肿瘤体积缩小≥75%的患者归为完全缓解/未确定,需要进行后续扫描。
(18F)氟脱氧葡萄糖PET扫描等功能性核影像学检测手段的出现进一步提高了对缓解的精确定义能力,能够识别出任何残留肿块中活跃的淋巴瘤或残留淋巴瘤的消失。PET扫描(以及后来的 PET/CT 扫描)纳入修订后的反应标准,并淘汰了完全缓解/未确定。PET扫描必须解决的问题在于,扫描下多大的摄取量与缓解相一致。在实现优化之前,将PET扫描加入反应标准中主要是基于其与CT扫描相比的优势。鉴别活动性淋巴瘤的方法已编入反应标准,并发展出应用于EOT PET扫描的5分Deauville评分,1-3 分为阴性,与完全缓解一致,而 4-5 分为阳性,与残留的活动性淋巴瘤一致。然而,EOT PET 扫描结果为阴性的患者中15% - 20%会复发,而许多 EOT PET 扫描结果为阳性的患者实际上并没有活跃淋巴瘤,即便未接受额外治疗也不会出现病情进展。在一项纳入 1418 例接受一线治疗的侵袭性 B 细胞淋巴瘤患者的随机 3 期研究中,EOT PET 扫描结果对无进展生存期(PFS)具有预后意义,对总生存期(OS)也有预后意义,但EOT PET 预测 2.5 年内进展或死亡的阳性预测值(PPV)低于 50%;此外20% 的缓解患者在治疗后复发或死亡,EOT PET 的阴性预测值(NPV)仅为 84%。其他针对侵袭性 B 细胞淋巴瘤的随机前瞻性研究也未证明 EOT PET 扫描具有任何预后价值。PET扫描无法可靠地区分活跃淋巴瘤和伴随免疫治疗可能出现的肿瘤炎症(称为假性进展),从而体现了其对淋巴瘤缺乏特异性,也因此专门开发了用于解读免疫治疗后PET扫描的单独反应标准。综合来看,这些数据强调了当前反应标准在定义侵袭性B细胞淋巴瘤缓解时的不精确性。
这些不确定性也反映在实践指南中,指南建议在EOT进行额外检查以确认疾病是否活跃,然后再进行挽救治疗(图 1)。约 75% 的患者对一线治疗有完全反应,但约15%的患者会复发,这促使通过定期门诊随访和/或影像学检查来监测复发情况,以便在出现症状前发现复发,但没有数据表明在出现复发症状前开始挽救治疗能带来更好预后。与之相反,约 25% 的患者对一线治疗没有完全反应,但这并不足以证明疾病处于活跃状态。指南建议在开始挽救治疗前进行额外的检查,如组织活检或重复PET扫描,但目前尚无数据表明在EOT进行额外检查的频率,而这些检查会增加医疗成本,并延误疾病活跃患者的挽救治疗。目前也不清楚有多少患者在未确认疾病活跃的情况下就接受了挽救治疗。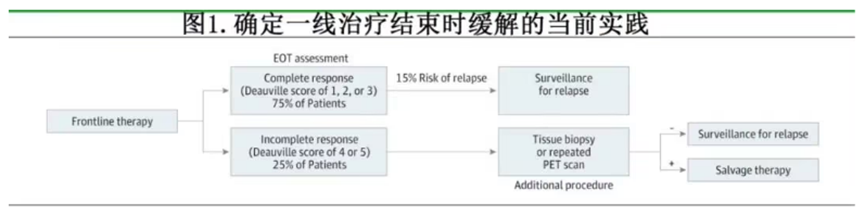
循环肿瘤DNA的出现
在血液系统治疗中,定义缓解的***新方法涉及到实验室检测手段,且多种方法已得到测试。在白血病中,检测循环肿瘤细胞是有效的,但侵袭性 B 细胞淋巴瘤细胞通常不会在外周血中循环。肿瘤特异性游离 DNA(cfDNA)或循环肿瘤 DNA(ctDNA)在血浆中的检测比在循环白细胞中更容易,已成为侵袭性淋巴瘤液体活检样本的***分析物。
在开发血液检测方法用于检测侵袭性 B 细胞淋巴瘤中MRD的时,面临的首要挑战在于特异性,而这一问题又因潜在的遗传异质性而变得复杂化。与由单一癌基因变异驱动的癌症不同,侵袭性 B 细胞淋巴瘤具有遗传复杂性,且患者间存在差异,因此仅针对单一基因变异进行检测是远远不够的。必须将源自恶性细胞的可检测异常与正常细胞凋亡、增殖和坏死自然释放到外周血液中的降解cfDNA片段区分开来,同时也要与克隆性造血区分开来,克隆性造血是指随着年龄增长而越来越频繁出现的造血细胞克隆性扩增。在血浆 DNA 中检测到的信号出现假阳性的机制至少有两种:该信号可能来自死亡且无法增殖的肿瘤细胞,也可能来自少量的存活肿瘤细胞,这些细胞***终会被宿主防御机制清除。目前还无法区分源自无增殖能力的濒死细胞的淋巴瘤序列和源自具有复发能力的克隆细胞的淋巴瘤序列。此外,ctDNA还面临单次 10 毫升血液样本(相当于 4 至 6 毫升血浆)中cfDNA含量过少以及外周血单个核细胞裂解可能造成 cfDNA 污染的挑战。由于血浆中的 DNA 污染水平较低,因此相较于血清,血浆更受青睐;若条件允许,使用能进一步降低污染风险的细胞稳定管则更佳。所有 ctDNA 检测的首要目标都是准确区分肿瘤特异性片段与背景 cfDNA。第二个主要挑战在于检测方法的分析灵敏度。在治疗前,ctDNA 检测方法的分析灵敏度可能不是关键问题,多种方法均有效,然而在治疗开始后,ctDNA 水平迅速下降,分析灵敏度就成为治疗中间时间点MRD检测的关键决定因素,在EOT中非常重要。
DNA提取磁珠可以有效的从标本中提取基因组DNA、病毒DNA或游离DNA,采用化学合成的方法将四氧化三铁进行特殊的处理,使其粒径达到均一化分散,再通过特殊的材料进行官能基团(如硅羟基、羧基)的包覆。包覆官能基团后,磁珠具备了核酸吸附能力,配合核酸提取仪,可以自动化的提取DNA和RNA。