联 系 人:吉恩特客服
手 机:136-0866-9917(微信同号)
地 址:河南省洛阳市高新区火炬创业园
在众多调节痛觉的心理和生理因素中,急性应激被认为是***有效的内源性镇痛因素之一。大量临床报道表明,即使在严重创伤条件下,个体在急性应激状态中仍可表现出显著的痛觉抑制效应。研究表明,中脑导水管周围灰质和吻侧腹内侧延髓 (rostral ventromedial medulla, RVM) 构成经典的镇痛调控系统,这些区域通过向脊髓发出下行投射来抑制伤害性信号向***脑区的传递。然而,该下行调控如何在脊髓层面实现对痛觉输出的调控仍不明确。
苏黎世大学与苏黎世联邦理工学院Zeilhofer教授团队在Neuron杂志在线发表题为"GABAergic Gbx1 neurons of the superficial dorsal horn are critical elements of a spinal circuit for stress-induced analgesia"的研究论文,系统解析了急性应激镇痛的脊髓环路机制。研究发现,急性应激通过调控来自RVM的下行GABA能输入,解除对脊髓背角GABA能神经元的tonic 抑制,形成去抑制环路。该过程特异性激活位于脊髓浅层背角的Gbx1阳性GABA能神经元亚群,直接抑制投射至外侧臂旁核(PbN)的伤害性输出神经元,有效阻断疼痛信号向***脑区的传递。 
01 浅层背角Gbx1神经元介导急性应激诱导的镇痛效应
研究者通过基因工具小鼠Gbx1-cre结合注射AAV8.hSyn.flex.DREADD的策略,实现Gbx1神经元的特异性操控。***游泳应激后小鼠在冷板、Hargreaves热辐射和针刺测试中均表现出显著的痛阈提升。随后向Gbx1-cre小鼠腰髓注射AAV8.hSyn.flex.hM4Di-mCherry以抑制脊髓Gbx1神经元,取消了游泳应激诱导的镇痛作用。
为进一步区分浅层与深层的作用,向Gbx1cre;GlyT2::Dre双转基因小鼠腰髓注射Cre/Dre双依赖AAV8.ConDon.hM4Di-mCherry,特异性沉默深层背角GlyT2阳性Gbx1神经元。结果显示,化学遗传学抑制深层Gbx1神经元不影响急性游泳应激诱导的镇痛效应,提示脊髓浅层背角Gbx1神经元是介导应激诱导镇痛的关键类型。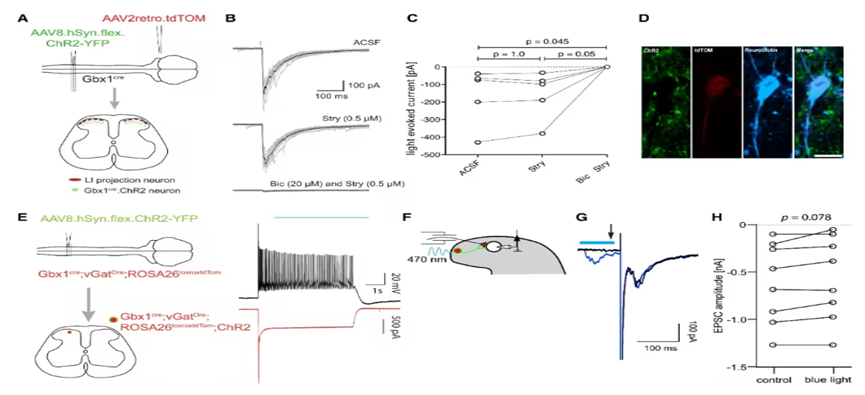
研究者采用逆行跨突触示踪技术研究脊髓Gbx1神经元的输入核团。检测发现Gbx1神经元的输入神经元广泛分布于延髓、中脑、脑桥、丘脑及大脑皮层。其中延髓RVM区域神经元占比***高。多重荧光原位杂交(mFISH)结合逆行标记结果显示,RVM输入神经元中约72%表达vGat,70%表达Gad2,59%表达Gad1,49%表达GlyT2,表明脊髓Gbx1神经元主要接收来自RVM的抑制性(GABA能/甘氨酸能)输入。
生物磁珠对细胞筛选的方法已日渐成熟,原理是将包被一抗的磁珠与细胞表面对应的分子特异性结合,或者将包被二抗的磁珠与已经与细胞表面分子特异性结合的一抗结合。磁珠携带与之结合的细胞吸附与分离柱或试管上,实现阳性细胞或阴性细胞的分离。洛阳吉恩特生物自主研发生产了各类生物磁珠,可以实现稳定的实验结果。