联 系 人:吉恩特客服
手 机:136-0866-9917(微信同号)
地 址:河南省洛阳市高新区火炬创业园
微生物群作为癌症免疫治疗的关键调节因子,正日益成为改善免疫检查点抑制剂疗效与安全性的重要研究方向。越来越多的证据表明,肠道与肿瘤微生物群可通过调节树突状细胞、T细胞功能及肿瘤微环境,深刻影响免疫治疗的应答与耐受,微生物群失调与免疫相关不良事件的发生密切相关,凸显其在治疗中的双重调控作用。基于此,靶向微生物群的干预策略——如粪便微生物群移植、工程菌及膳食调节——在临床前与早期临床研究中已显示出增强免疫治疗应答、减轻毒副反应的潜力。然而,其临床转化仍面临机制复杂性、个体差异及标准化方案缺乏等挑战。《Seminars in Cancer Biology》(IF:15.7)上发表了题为《Microbiota and cancer immunotherapy: Mechanisms, clinical implications, and precision therapeutics》的综述。该文系统阐述了微生物组-免疫-肿瘤相互作用的机制基础,总结了微生物干预在免疫治疗中的临床意义,并探讨了迈向精准微生物治疗所面临的科学与转化瓶颈。文章强调,通过整合微生物组分析、宿主因素与肿瘤特征,可构建个体化免疫治疗新策略,从而推动精准肿瘤学向微生物调控纵深发展。
微生物组研究的***新进展揭示,通过复杂的宿主-微生物相互作用,微生物失调既可促进也可抑制肿瘤发展。这使得微生物组成为解读宿主-环境-免疫轴的变革性视角,已有证据表明微生物群落与免疫检查点抑制剂(ICIs)的疗效及毒性存在关联。目前正积极探索以微生物组为靶点的干预手段——包括益生菌、益生元、饮食调整、粪便微生物群移植(FMT)、工程化益生菌及溶瘤病毒疗法——以增强免疫疗法效果并减少治疗相关并发症。然而挑战依然存在,例如微生物组研究中因果关系与相关性的辨析,以及微生物代谢途径中物种间变异性的理解。因此,本综述旨在探索微生物组与癌症免疫疗法之间的机制关联,评估现有治疗策略,并探讨如何利用微生物生态学改善癌症治疗效果的未来方向。 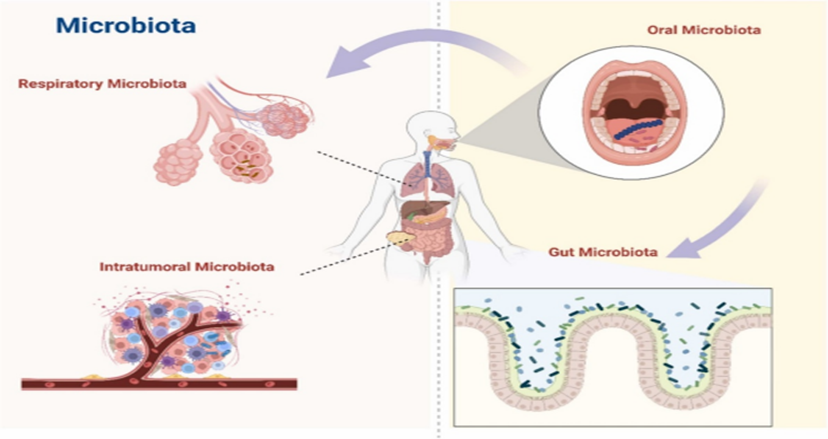
图1.人类微生物群:一个超级器官系统
核梭杆菌(F. nucleatum)是牙周病橙色复合体的成员,在口腔鳞状细胞癌(OSCC)患者中大量存在,其在免疫治疗中的作用仍具争议性,可能取决于癌症类型及微环境。核梭杆菌可通过上调 OSCC 中凝集素-9 和 PD-L1 的表达介导肿瘤免疫逃逸,该过程进一步诱导 PD-L1 的表达,导致胃癌中 CD8⁺ T 细胞耗竭并促进免疫逃逸。在结直肠癌患者中,核梭杆菌在肿瘤组织中的丰度显著高于健康人群。一项针对结直肠癌患者的研究发现,免疫治疗应答者体内核梭杆菌阳性率显著升高,该菌通过 STING 信号通路上调 PD-L1 表达,动物模型实验表明其联合抗 PD-L1 治疗可显著抑制肿瘤生长。核梭杆菌可产生丁酸盐,该物质通过抑制 HDAC3/8 并增强 Tbx21 启动子区域 H3K27 乙酰化水平,上调 TBX21(T-bet)表达。此过程直接抑制 PD-1 表达,缓解 CD8⁺ T 细胞耗竭状态,增强其细胞毒性功能(图2)。
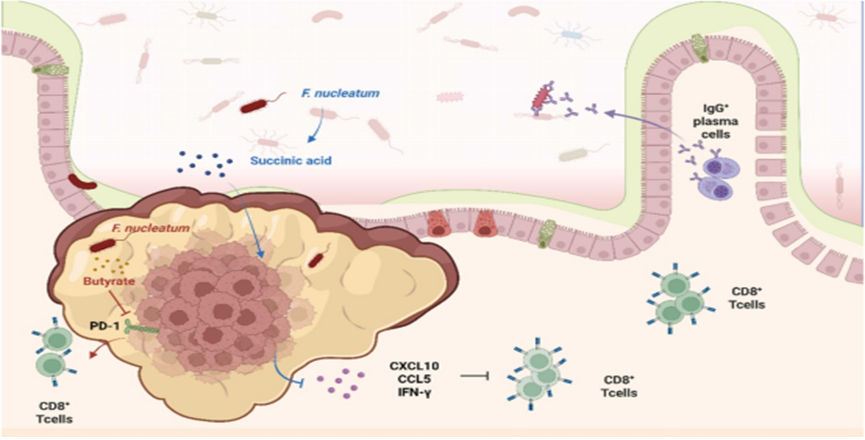
图2. 核梭杆菌对免疫疗法的影响
在另一组研究中,观察到了相反的结果。对免疫治疗无反应的患者,其粪便和肿瘤组织中的核酸杆菌丰度均显著升高,核酸杆菌产生的琥珀酸可与SUCNR1 受体结合,抑制 Th1 型趋化因子的表达,这种下调效应进而阻碍了 CD8⁺ T 细胞向肿瘤微环境的招募。在接受 PD-1 抑制剂治疗的食管鳞状细胞癌患者中,非应答组的肿瘤组织和血清中核酸杆菌丰度显著高于应答组。该菌的致病因子转运至细胞核并与转录因子 ATF3 结合,显著上调肿瘤细胞表面的 PD-L1 表达。然而在小鼠模型中,核酸链霉菌感染显著削弱了免疫疗法的抗肿瘤效果。
变形链球菌同样是口腔微生物组中的重要菌种。定植于肿瘤的变形链球菌可介导色氨酸代谢产物犬尿氨酸的生成,该物质能促进 S100a8 高表达 / S100a9 高表达中性粒细胞扩增以产生更多白细胞介素-1β,诱导 CD8⁺ T 细胞耗竭,并在动物模型中削弱免疫治疗的效果。
DNA提取是分析农作物分子生物学性状的重要步骤,现阶段,常用的DNA提取技术有磁珠法和离心柱法,使用磁珠进行农作物的DNA提取,可以实现高通量、自动化的操作。由于磁珠对核酸的吸附灵敏度高,只需要少量的叶片或其他组织即可得到高得率、高纯度的DNA。吉恩特生物采用自主研发生产的纳米生物磁珠和磁珠法DNA提取试剂盒,可以从各种类型的农作物中提取高质量的核酸,配合核酸提取仪,可以达到快速自动化提取的目的。