联 系 人:吉恩特客服
手 机:136-0866-9917(微信同号)
地 址:河南省洛阳市高新区火炬创业园
遗传性耳聋指的是由于基因和染色体异常所致的耳聋。这种疾病是由父母的遗传物质(包括染色体及位于其中的基因)发生了改变传给后代而引起的耳聋,并且在于孙后代中以一定数量出现。在每1000个新生儿中就有一位患有先天性耳聋,其中60%以上是由遗传因素引起的,遗传性聋的群体发病率已超过27/1000,在所有耳聋病人中,遗传性聋约占50%。遗传性聋分为综合征性遗传性聋及非综合征性遗传性聋两大类。前者指除了耳聋以外,同时存在眼、骨、肾、皮肤等部位的病变,这类耳聋占遗传性聋的30%;后者只出现耳聋的症状,在遗传性聋中占70%。
其中一部分病人,在出生后就对声音没有反应,如果不配戴助听器和接受语言训练,不但无法进行正常的交流,而且还阻碍了聋儿正常的智力发育,成为家庭和社会沉重的负担;另一部分病人,只在10~30岁之间发病,表现为听力下降,并随着年龄增加不断加重,以至达到极重度耳聋,这类病人虽然己学会说话,但由于听力障碍,不能和别人进行正常的语言交流,也不能像正常人那样看电影、电视,听广播、音乐,对本人和家庭都是个极大的痛苦
随着现代科学技术的进步以及分子遗传学的飞速发展,人们对遗传性聋的认识不断加深,阻止遗传因素导致耳聋的技术离实现临床已越来越近。
近日,哈佛大学医学院耳鼻喉科副教授 Zheng-Yi Chen 和哈佛大学化学与化学生物学教授、美国博德研究所核心成员 David R. Liu 共同主导的一项研究在线发表在在国际***期刊《自然》(Nature),该团队用基因编辑技术治疗 TCM1 突变“贝多芬小鼠”的遗传性耳聋,并取得良好效果。
内耳是声音感知的***重要部位,其中内耳毛细胞又是人类听到声音的关键。其中,TCM1 是内耳毛细胞中机械力传导的重要组成部分,TCM1 蛋白在内耳毛细胞的纤毛上形成通道,当声波引起纤毛运动时这种通道就会打开,随后钙离子进入细胞生成电信号,电信号传递到大脑后形成听觉。
TCM1 发生了一种显性负性错义突变后,会导致内耳毛细胞单通道电流水平和钙渗透率降低,进一步导致感音神经性语后聋(语言形成后出现耳聋)。通常,TCM1 显性突变患者在 10-15 岁时会开始逐渐变聋。
TCM1 显性突变即意味着,一对等位基因中只有一个发生突变就会导致功能丧失,从而致聋。这也就使得修复显性突变成了一项精细的任务:必须使突变基因失活,同时还要保留野生型基因。这一对基因的差别只在于其中一个核苷酸的不同。突变的 TCM1 在原本野生型一个胸腺嘧啶核苷酸 T 的位置变成了腺嘌呤核苷酸 A。
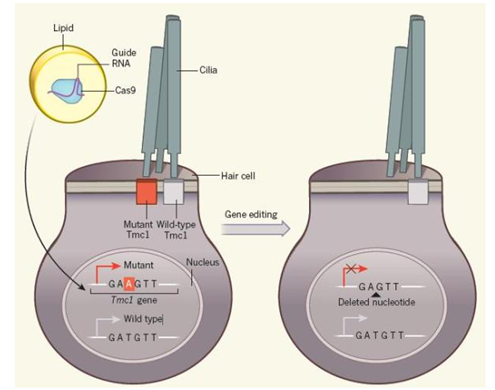
基因编辑过程示意图
Chen 和 Liu 团队启用的是热门的 CRISPR–Cas 基因编辑技术。研究团队将含有 Cas9 和 RNA 的脂滴注入新生 TCM1 贝多芬小鼠的内耳,这种脂滴能和细胞随后融合。基因编辑后突变基因中腺嘌呤核苷酸 A 被敲除,从而使该基因失活。但同时保留了野生型基因,保证正常听力功能实现。
研究团队评估得出,基因编辑过的小鼠中内耳毛细胞的存活率更高、听脑干反应阈值更低。此外,听觉反射也出现改善,基因编辑过的成年贝多芬小鼠在听到突发噪音时会表现出惊吓,然而未经基因编辑的小鼠对此毫无反应。
这一治疗途径在治疗和内耳毛细胞功能障碍有关的常染色体显性遗传耳聋方面具备潜力,也为反义寡核苷酸疗法和 RNA 干扰疗法提供了补充策略。